生物技术药物发展迅猛,突破性疗法认证推动药
2017年是新药研发领域取得重要突破与进展的一年:肿瘤免疫疗法热度不减,免疫检查点抑制剂再添新成员,全球首款细胞免疫CAR-T疗法正式获批上市,全球首个按生物标记物而非肿瘤来源区分的抗肿瘤疗法获批,基因编辑技术快速发展助力新药研发,基因治疗迎来新进展前景可期;人工智能领域的突破性进展或为新药研发领域注入新活力,革新新药研发现状。此外,2017年又是新药研发领域成果丰硕的一年:美国食品药品监督管理局(FDA)新药获批数量创历史新高,突破性疗法认证推动药物创新,多个全球首款药物加速获批;在中国,国家食品药品监督管理总局(CFDA)改革新政频出,鼓励创新接轨国际,新药研发迎来重大发展机遇,也面临更多挑战。
肿瘤治疗领域迎来新突破
2017年初,美国癌症学会发表了《2017年癌症统计年度报告》,报告指出,在过去20余年中,美国的癌症总死亡率下降了25%,这主要得益于肿瘤治疗领域科学的发展。近年来,在肿瘤治疗领域,人们越来越多地致力于利用自身免疫系统来抵御肿瘤,这种通过调动机体免疫系统,抑制和杀伤肿瘤细胞的方法称为肿瘤免疫治疗。肿瘤免疫治疗是当前肿瘤治疗领域中最具前景的研究方向,包括细胞免疫疗法、肿瘤疫苗及免疫检查点抑制剂等研究热点,当前已取得了很多具有应用前景的研究成果(图1)。2017年,肿瘤免疫疗法迎来新突破,免疫检查点PD-1/PD-L1抑制剂又添新丁,细胞免疫CAR-T疗法首次获批上市。此外,首款按生物标记物而非肿瘤来源区分的肿瘤个性化药物获批,成为里程碑式的新进展,为肿瘤治疗领域带来新希望。
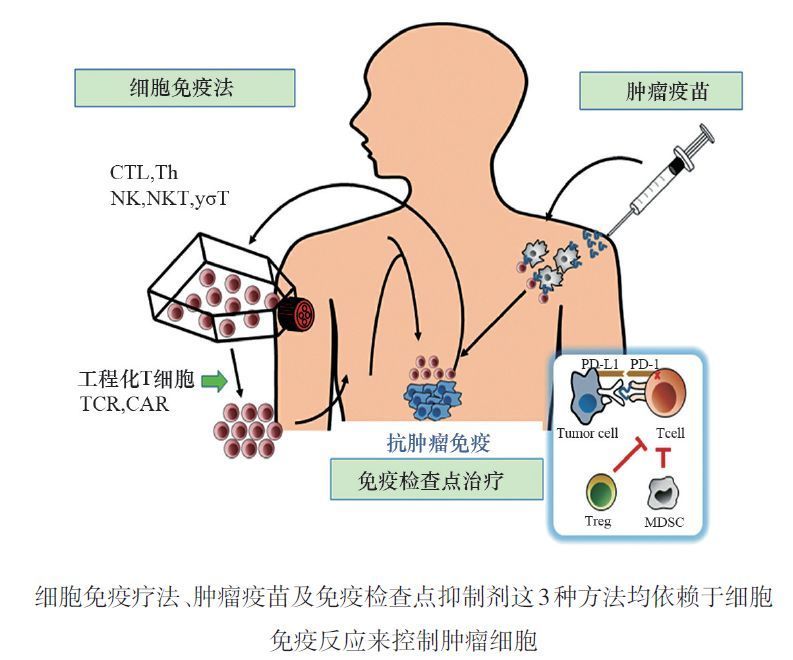
图1 肿瘤免疫疗法示意
PD-1/PD-L1抑制剂再添新成员
免疫检查点(immune checkpoint)是指免疫系统中存在的一些抑制性信号通路,如细胞毒T淋巴细胞相关抗原4(Cytotoxic T-lymphocyte Associated Antigen-4,CTLA-4)、细胞程序性死亡受体1(Programmed Death1,PD-1)和细胞程序性死亡配体1(Programmed Death Ligand-1,PD-L1)。机体在正常情况下,免疫检查点可以通过调节自身免疫反应的强度来维持免疫耐受,但机体在受到肿瘤侵袭时,免疫检查点的激活可抑制自身免疫,有利于肿瘤细胞的生长和逃逸。其中,PD-1是一种诱导表达于活化的T细胞、B细胞和NK细胞等表面的共刺激分子,2个天然配体分别为PD-L1和PD-L2,表达于肿瘤细胞和抗原递呈细胞。激活PD-1/PD-L通路对已活化的T细胞有反向调控作用,降低T细胞活性,甚至诱导其凋亡。反之,阻断PD-1/PD-L通路可以增强T细胞活性以达到肿瘤免疫治疗的效果。PD-1/PD-L1抑制剂是近年来肿瘤免疫治疗的重点研发领域,目前获批的肿瘤适应症包括黑色素瘤、非小细胞肺癌、肾细胞癌、膀胱癌等。2017年FDA又批准了两个PD-L1抑制剂,分别是默克/辉瑞的Bavencio(avelumab)和阿斯利康的Imfinzi(durvalumab)。截至目前,共有6个免疫检查点抑制剂获批上市(表1)。
表1 美国FDA批准上市的免疫检查点抑制剂

尽管当前PD-1/PD-L1抑制剂的研究如火如荼,但最新的研究进展却给这一方向敲响了警钟:抑制PD-1蛋白可激活T细胞启动针对肿瘤细胞的免疫应答,但是小鼠研究表明,这种免疫疗法加剧了T细胞参与的癌症进程;PD-1抑制剂对T细胞非霍奇金淋巴瘤(Tcell non-Hodgkin lymphomas,T-NHL)非但没有改善,反而有恶化效果,小鼠体内试验结果显示,基因敲除PD-1或使用PD-L1抑制剂都显著缩短T-NHL小鼠的寿命;在2017年癌症免疫治疗学会年会上,耶鲁大学免疫学专家Kevan Herold指出,免疫检查点抑制剂在挽救癌症病人生命的同时会引起诸如甲状腺疾病、结肠炎和1型糖尿病等疾病的快速发病,或是源于对患者自身组织的免疫攻击。因此,免疫检查点抑制剂的应用应考量药物剂量与准确度、用药周期等因素,针对不同的肿瘤类型、不同患者的特殊生物标记物开展联合用药。当前,多个
文章来源:《生物技术》 网址: http://www.swjszz.cn/zonghexinwen/2020/1111/477.html